<출처>
https://ko.bccrwp.org/compare/difference-between-mole-fraction-and-weight-percent/
몰 분율과 무게 백분율의 차이
몰 분율과 중량 퍼센트의 주요 차이점은 몰 분율이 혼합물로 물질의 조성을 몰에 의해 제공하는 반면 중량 퍼센트는 조성물을 질량에 의해 제공한다는 점이다.
몰 분율 및 중량 퍼센트 또는 질량 분율은 혼합물에서 성분의 조성을 표현하는 두 가지 다른 방식이다. 이 두 값은 같지 않지만 결정 방법은 비슷합니다. 두 현상에서 원하는 성분의 몰수 또는 질량을 혼합물의 총 몰수 또는 총 질량으로 나눠 값을 구해야하기 때문에 . 일반적으로 중량 백분율은 백분율 값으로 표시됩니다.
내용
1. 개요 및 주요 차이점 2. 몰 분율이란? 3. 중량 퍼센트 란? 4. 나란히 비교 – 표 형태의 몰 분율 대 중량 퍼센트 5. 요약
두더지 분수 란 무엇입니까?
혼합물 중의 성분의 몰 분율은 성분의 몰수를 혼합물의 총 몰수로 나눈 값이다. 이 값은 혼합물에 존재하는 특정 성분의 양 (몰에 의한 성분의 조성)을 나타냅니다. 일반적으로이 값은 분수 또는 소수 자릿수 또는 소수 자릿수로 제공됩니다. 비율이기 때문에 몰 분율은 단위가 없습니다.
혼합물에서 각 성분의 몰 분율을 결정할 수 있으며, 이러한 분율 값을 더하면 1이됩니다. 염 용액에 2 몰의 염화나트륨 및 5 몰의 물을 함유하는 혼합물이있는 경우, 총 몰수는 2 + 5 = 7이다. 여기 염화나트륨의 몰 분율을 계산해야한다면
염화나트륨의 몰 분율 = 혼합물에서 염화나트륨의 몰 / 총 몰
= 2 / (2 + 5)
= 2/7
= 0.28
무게 백분율은 무엇입니까?
중량 퍼센트 또는 질량 퍼센트는 혼합물 중 성분의 질량 퍼센트이다. 우리는 이것을 질량 분율이라고 부릅니다. 또한,이 용어는 원하는 성분의 질량과 혼합물의 총 질량에 100을 곱한 비율을 백분율 값으로 얻는다. 이 결정의 공식은 다음과 같습니다.
중량 퍼센트 = (성분의 질량 / 혼합물의 총 질량) * 100
질량 백분율의 표시는 (w / w) %입니다.
위의 공식은 질량 백분율에 대한 일반적인 아이디어를 제공하지만 공식의 적용은 구성 요소의 유형과 처리하는 혼합물에 따라 다릅니다. 예를 들어
화합물의 화학 원소의 경우 질량 백분율은 다음과 같이 계산됩니다.
중량 퍼센트 = (화합물 1 몰당 원소의 질량 / 몰 몰) * 100
용액의 용질의 경우
중량 퍼센트 = (용질의 그램 / 용질과 용매의 그램) * 100
몰 분율과 중량 퍼센트의 차이는 무엇입니까?
몰 분율 및 중량 백분율은 혼합물 중 성분의 농도를 표현하는 두 가지 다른 방법이다. 몰 분율과 중량 퍼센트의 주요 차이점은 몰 분율이 혼합물로 물질의 조성을 몰에 의해 제공하는 반면, 중량 백분율은 조성물을 질량에 의해 제공한다는 점이다. 또한, 몰 분율의 값은 분수 또는 소수점 이하 한 자리 또는 두 자리로 주어지며 무게 백분율은 백분율 값으로 제공됩니다.
아래의 인포 그래픽은 몰 분율과 중량 퍼센트의 차이를 요약합니다.
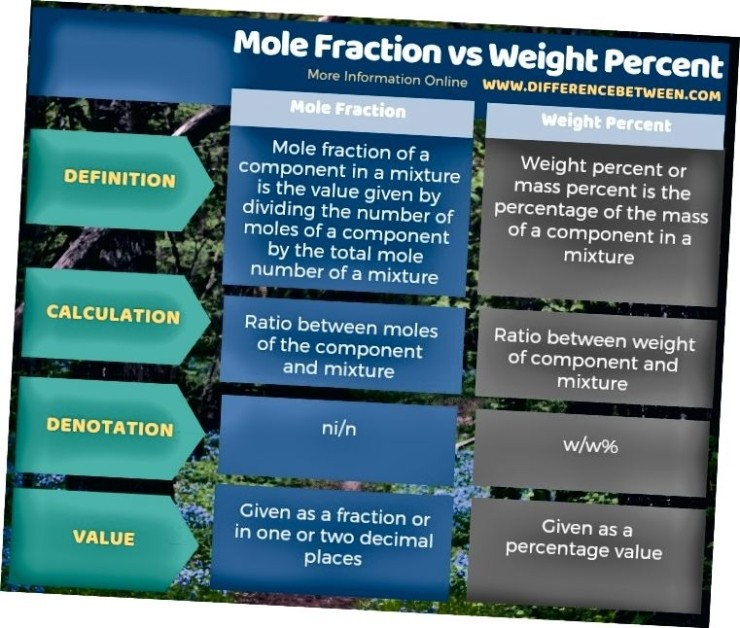
표 형태의 몰 분율과 중량 백분율의 차이(요약 – 몰 분율 대 중량 백분율)
몰 분율 및 중량 백분율은 혼합물 중 성분의 농도를 표현하는 두 가지 다른 방법이다.
몰 분율과 중량 퍼센트의 주요 차이점은 몰 분율이 혼합물로 물질의 조성을 몰에 의해 제공하는 반면, 중량 백분율은 조성물을 질량에 의해 제공한다는 점이다.
'교육과 학습' 카테고리의 다른 글
| 초등학교 3학년 2학기 과학 5단원 소리의 성질 (0) | 2020.12.01 |
|---|---|
| 아시아태평양 영재성 학회 2020 (0) | 2020.11.30 |
| how to padlet 패들렛 사용법 모음 (0) | 2020.11.09 |
| 줌과 파워포인트 활용하여 동영상 강의 만들기 필수 강좌 모음 (0) | 2020.11.09 |
| 계절이 없다면 지구는 어떤 모습일까? (0) | 2020.10.22 |
